Tous les médicaments que nous utilisons, qu'il s'agisse de traitements communs ou de traitements plus spécialisés, ont été découverts grâce à la recherche. Par exemple, la recherche clinique a permis de développer les médicaments utilisés pour le traitement du cancer, des maladies cardiovasculaires, du diabète, etc. Il faudra environ 15 ans aux chercheurs pour développer un traitement sécuritaire et efficace pour chacune des maladies (voir figure).
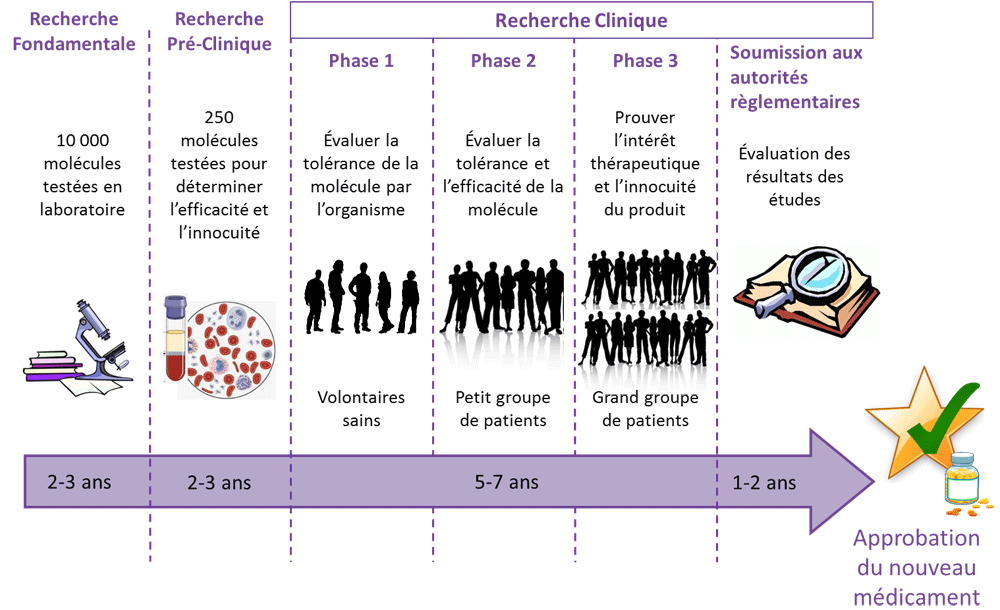
Les différentes étapes du développement d'un médicament.
La recherche clinique s'appuie sur les résultats de la recherche fondamentale afin de développer de nouveaux traitements, des dispositifs ou des actes médicaux et d'en évaluer l'efficacité. En phase pré-clinique, la recherche est effectuée par des laboratoires universitaires ou pharmaceutiques, sur des modèles biologiques (tests in-vitro) ou animaux (tests in-vivo). L'objectif est d'identifier de nouvelles molécules pour les utiliser plus tard chez les humains de façon efficace et sécuritaire. Lorsque les chercheurs pensent avoir trouvé un traitement efficace, on passe aux étapes de la recherche clinique.
Méconnue du grand public, la recherche clinique représente pourtant un enjeu majeur de santé. En effet, c'est une étape indispensable dans le développement de nouveaux traitements et de médicaments innovateurs. Il faut noter que la recherche clinique est strictement encadrée par la loi et ne peut se dérouler que dans des conditions bien précises.
Une étude clinique consiste à tester sur l'homme un médicament, un dispositif médical, ou un acte médical, afin d'évaluer quels bénéfices il peut apporter et quels risques il peut comporter. L'étude clinique peut également porter sur un traitement déjà existant dans le but de l'améliorer ou de le comparer avec un autre traitement. L'étude clinique est une des dernières étapes de la mise au point d'un nouveau traitement.
La recherche médicale contribue à la découverte de nouveaux traitements et à l'amélioration des connaissances sur les maladies.
Trois phases d'études cliniques seront nécessaires pour qu'un nouveau médicament soit approuvé pour le traitement d'une maladie :
• La phase 1 a pour but d'évaluer la tolérance de la molécule par l'organisme. Elle est effectuée sur de petits groupes de participants, en général des volontaires sains, c'est-à-dire des personnes qui ne sont pas affectées par la maladie pour laquelle la molécule testée est destinée.
• La phase 2 permet d'évaluer la tolérance et l'efficacité de la molécule. Elle est effectuée sur de petits groupes de participants atteints de la maladie à traiter. Elle se déroule en général en milieu hospitalier afin qu'une surveillance médicale étroite des participants puisse avoir lieu.
• La phase 3 a pour but d'apporter la preuve de l'intérêt thérapeutique du produit testé et de son absence de nocivité. Elle est conduite sur un grand nombre de participants malades (jusqu'à plusieurs milliers de personnes). Cette phase constitue la dernière étape avant que le médicament soit disponible pour les patients.
Avant de pouvoir débuter, toute étude clinique est soumise aux autorités réglementaires du ou des pays où elle sera effectuée. Leur approbation est obligatoire pour effectuer l'étude. De plus, elle est évaluée par un comité d'éthique qui a pour rôle de s'assurer que le protocole à l'étude respecte la sécurité des participants et les lois en matière de recherche clinique. Il prend en compte, entre autres, la pertinence de la recherche, l'adéquation entre les objectifs et les moyens mis en œuvre ainsi que la qualité des informations délivrées aux personnes y prenant part pour recueillir leur consentement. Les comités d'éthique sont constitués de professionnels de la santé, de membres de la collectivité, de représentants éthiques, de représentants légaux et de toute autre personne possédant une expertise précise. Une approbation du comité d'éthique est obligatoire pour pouvoir démarrer une étude clinique.
La participation aux études cliniques se fait sur une base volontaire et il est toujours possible de retirer son consentement à participer sur simple avis verbal et ce, sans aucun préjudice. Bien que la participation à la recherche clinique soit potentiellement ouverte à tous, chaque étude clinique comporte des critères d'inclusion et d'exclusion spécifiques. Les critères d'inclusion décrivent les caractéristiques que doivent présenter les participants, tandis que les critères d'exclusion décrivent les caractéristiques qu'ils ne doivent pas présenter pour pouvoir participer à un essai clinique. Lorsque vous participez à un projet de recherche, on vous attribue dès votre première visite un numéro de participant, afin qu'il ne soit pas possible de vous identifier. Votre confidentialité est ainsi protégée.
Les participants aux études cliniques sont des acteurs majeurs de la réussite de la recherche médicale. Il n'y a pas de bénéfice direct garanti pour vous en raison de votre participation à une étude. Toutefois, si le traitement s'avère efficace, cela aidera à l'avancement des connaissances scientifiques dans ce domaine.
En 2000, 25% des décès ont été attribués aux maladies cardiaques au Canada. Ce pourcentage a diminué à 20% en 2011. Cette amélioration est attribuée entre autre à la recherche médicale effectuée au cours des dernières années.
